Molekulare und zelluläre Funktionsweisen von Naturstoffen
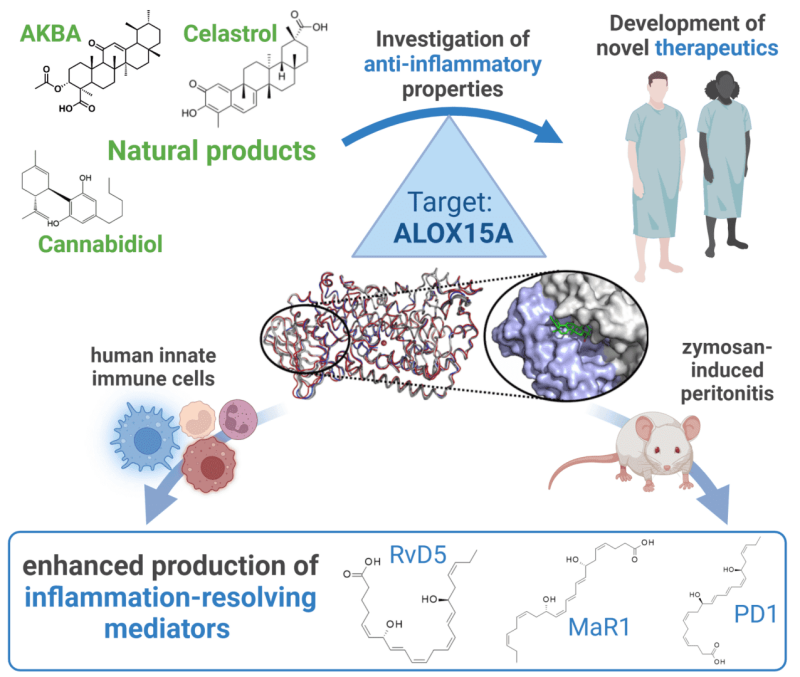
Charakterisierung von Naturstoffen zur aktiven Auflösung von Entzündungen
Foto: Paul JordanBei den Naturstoffen handelt es sich um Inhaltsstoffe aus Arzneipflanzen wie Triterpensäuren (Boswelliasäuren, Tirucallensäuren, Lupansäuren etc.) aus dem Weihrauchharz (Boswellia-Arten), Acylphloroglucinole (z.B. Hyperforin, Myrtucommulon, Garcinol, Arzanol, etc.), Curcuminoide, Cannabinoide und Indirubin-Derivate, sowie um Naturstoffe aus Bakterien und Pilzen (z.B. α-Hemolysin, Gliotoxin und Melleolide). Ziel ist die Identifizierung molekularer Zielstrukturen und der zugrundeliegenden molekular/biochemischen Mechanismen sowie die Klärung der pharmakologischen Relevanz der Wirkstoff-Target-Interaktion. In Kooperation mit anderen Arbeitsgruppen, werden Totalsynthesen ausgewählter Naturstoffe angegangen, um u. a. Substanzbibliotheken zur Struktur-Wirkungsoptimierung zu erstellen. Die molekularpharmakologische Evaluierung berücksichtigt wichtige in vivo-relevante Regulationsmechanismen und soll neue Möglichkeiten/Angriffsorte zur molekularen Interferenz mit den Zielstrukturen liefern. Diese Kenntnis dient einerseits der Entwicklung von Therapeutika und zum anderen neue Proteinfunktionalitäten in pathobiochemischen Prozessen zu enthüllen (Wirkstoffe als Werkzeuge).
Schlüsselpublikationen:
Peltner L., Gluthmann L., Börner F., Pace S., Hoffstetter R.K., Kretzer C., Bilancia R., Pollastro F., Koeberle A., Appendino G., Rossi A., Newcomer M.E., Gilbert N.C., Werz O.*, Jordan P.M.* (2023) Cannabidiol acts as molecular switch in innate immune cells to promote the biosynthesis of inflammation-resolving lipid mediators. Cell Chem. Biol., 30(12):1508-1524.
Börner F., Pace S., Jordan P.M., Gerstmeier J., Gomez M., Rossi A., Gilbert N.C., Newcomer M.E., Werz O. (2023) Allosteric activation of 15-lipoxygenase-1 by boswellic acid induces the lipid mediator class switch to promote resolution of inflammation. Adv Sci, 10(6):e2205604
Pace S., Zhang K., Jordan P.M., Bilancia R., Wang W., Börner F., Hofstetter K., Potenza M., Kretzer C., Gerstmeier G., Fischer D., Lorkowski S., Gilbert N.C., Newcomer M.E., Rossi A., Chen X., Werz O. (2021) Anti-inflammatory celastrol promotes a switch from leukotriene biosynthesis to formation of specialized pro-resolving lipid mediators. Pharmacol Res, 167:105556
Forschungsverbünde:
DFG SFB1127 „ChemBioSys“
DFG SFB1278 „Polytarget“
TAB-Forschergruppe “Nature4HEALTH“